El estudio, publicado en la revista Translational Neurodegeneration, describe los efectos funcionales de la proteína Galectina 3 (Gal-3) en la actividad de los circuitos neuronales del hipocampo –estructura involucrada en procesos de plasticidad sináptica y de aprendizaje y memoria, entre otras funciones– y plantea su inhibición para paliar el deterioro neurológico producido por la enfermedad de Alzheimer y otros trastornos neurodegenerativos relacionados con la inflamación del cerebro. El trabajo ha sido conducido por los investigadores Yuniesky Andrade Talavera y Antonio Rodríguez Moreno, del Laboratorio de Neurociencia Celular y Plasticidad de la Universidad Pablo de Olavide, en colaboración con André Fisahn, del Laboratorio de Oscilaciones Neuronales del Instituto Karolinska (Suecia). Han participado también investigadores de la Universidad de Sevilla y de la Universidad de Lund en Suecia.
El papel de la Galectina-3 en reacciones inflamatorias en el cerebro es conocido; esta proteína se encuentra alterada en modelos animales de enfermedades neurodegenerativas y en pacientes que sufren la enfermedad de Alzheimer, produciendo una amplificación de señales inflamatorias. Sin embargo, no se conocían sus efectos sobre la actividad de los circuitos neuronales involucrados en el procesamiento de la información que ocurre en estructuras cerebrales relacionadas con la memoria, como el hipocampo, cuya funcionalidad sufre un deterioro progresivo en la enfermedad de Alzheimer.
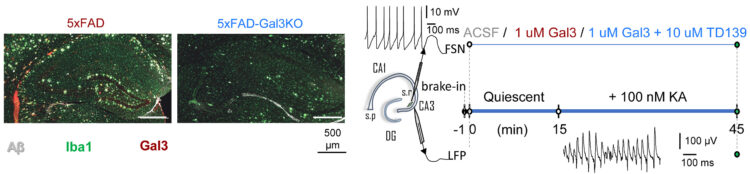
Realizando registros electrofisiológicos de la actividad neuronal de un área concreta del hipocampo (CA3) en estado basal e induciendo ritmos cerebrales (oscilaciones de tipo gamma) en el cerebro de ratones, el equipo de investigación ha observado que la Galectina-3 deteriora la comunicación eficiente entre las neuronas y su habilidad para producir oscilaciones gamma. Estos ritmos cerebrales están muy relacionados con el procesamiento de información y con funciones cognitivas superiores como la memoria.
Los efectos nocivos observados a nivel funcional en los circuitos neuronales estudiados se previenen al inhibir la Galectina-3. Así, el deterioro de las oscilaciones gamma observado en un modelo de la enfermedad de Alzheimer en un estado avanzado no se observó si el mismo modelo carece de señalización por Gal-3 y estos animales que carecen de dicha proteína no desarrollan el deterioro cognitivo típico de la enfermedad.
Posible diana terapéutica frente al deterioro cognitivo con un inhibidor aprobado por la FDA
El estudio destaca la importancia de centrar las estrategias terapéuticas en restablecer la funcionalidad de circuitos neuronales relacionados con funciones cognitivas utilizando la Galectina-3 como diana frente a la inflamación. Así, este camino comienza a dar frutos en el campo de la investigación preclínica en la enfermedad de Alzheimer en contraste con el bajo ratio de éxito de ensayos clínicos durante los últimos veinte años que se han centrado mayoritariamente en eliminar proteínas que se acumulan en el cerebro de los pacientes, como la beta amiloide.
Además, las oscilaciones neuronales comienzan a deteriorarse mucho antes de la expresión clínica de la enfermedad y, al menos en modelos de roedores, es posible recuperar formas de memoria con intervenciones dirigidas a restablecer dichas oscilaciones. Cabe destacar que el inhibidor de la Galectina-3 (TD139) usado en este estudio está aprobado por la FDA, agencia gubernamental de los Estados Unidos responsable en la regulación de medicamentos. Los investigadores señalan que estas estrategias podrían, probablemente, aplicarse al estudio de otros desórdenes neurodegenerativos que cursen con deterioro cognitivo relacionado con la inflamación del cerebro y deficiencias en la funcionalidad de circuitos neuronales claves.
Artículo de referencia:
Arroyo-García LE, Bachiller S, Ruiz R, Boza-Serrano A, Rodríguez-Moreno A, Deierborg T, Andrade-Talavera Y, Fisahn A. (2023) Targeting Galectin-3 to counteract spike-phase uncoupling of fast-spiking interneurons to gamma oscillations in Alzheimer’s disease. Transl. Neurodegener. 12(1):6. DOI: 10.1186/s40035-023-00338-0.